尿石素A (Urolithin A) 作为抗衰领域的前沿成分与天然多酚代谢产物,凭借其独特的细胞代谢调控机制,近年已成为科学界与产业界在睡眠改善与抗衰老领域的关注焦点。
邦尚健康作为专业的尿石素A原料生产商,始终坚持医药级标准生产高纯度原料,并秉持“科学先行”的研发理念,持续投入临床探索与验证。继2025年上半年成功完成首项口服美容临床实验后,我们第二项关于尿石素A改善睡眠质量的临床研究也已正式通过伦理审查并进入实施阶段。这项针对中老年人睡眠健康的随机平行四盲对照实验,不仅聚焦碎片化睡眠、昼夜节律失调等现代康问题,更旨在通过多维度生物标志物监测,系统性验证尿石素A在睡眠和抗衰领域的全谱健康价值。

一、睡眠危机:现代生活方式下的“衰老加速器”
数据显示,全球有30%~35%的成年人受困于睡眠障碍[1]。在数字化浪潮中,熬夜工作、碎片化娱乐、昼夜颠倒等生活方式已成为常态,由此引发的睡眠不足问题正成为从细胞、器官到系统层面加速人体衰老进程的“隐形杀手”。
01 碎片化睡眠:从“睡眠剥夺”到“细胞损伤”的级联反应
碎片化睡眠是一种常见的睡眠障碍,指在睡眠过程中由于外源和内源性因素导致的睡眠中断和觉醒,表现为睡眠不深且不连贯[2]。研究显示,约65.91% 的被调查者有此类睡眠困扰,其中,35~44岁年龄段人群的睡眠困扰率最高,达71.95%[3]。其危害远超单纯的疲劳感:
细胞代谢紊乱:睡眠中断会破坏肌细胞蛋白合成,增加心肌中的脂肪酸氧化和自由基ROS,同时在肝细胞中引发氧化应激,导致肝脏损伤[4]。
衰老细胞蓄积:慢性睡眠不足使细胞衰老标志物p16INK4a的表达在小鼠主动脉壁中显著增加,且细胞促炎因子IL-6增加约1倍,加速炎症和组织退化[5]。
代谢综合征风险:碎片化睡眠会增加机体胰岛素抵抗的发生率和血糖水平,与内脏脂肪堆积形成恶性循环[4]。
02 昼夜节律失调:当“生物钟”遭遇“光污染”
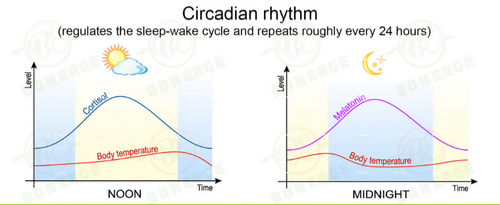
现代社会的光照环境(如蓝光暴露)与不规律作息,正系统性破坏人体昼夜节律。作为调控睡眠-觉醒周期的核心机制,昼夜节律通过视交叉上核(SCN)协调全身基因表达的24小时振荡[6]。研究表明,昼夜节律失调对健康的影响深刻而广泛:
时钟基因异常:夜班工作者的时钟基因PER1和BMAL1节律普遍延迟约2.5至3小时,进一步影响褪黑素分泌节律[7]。
炎症失控:节律紊乱使Th17细胞活化增强,IL-17A水平升高,与银屑病、类风湿关节炎等炎症性问题密切相关[8]。
NAD+代谢失衡:NAD+(烟酰胺腺嘌呤二核苷酸) 是维持细胞代谢和能量稳态的重要辅酶,而SIRT1蛋白是NAD⁺代谢的重要调控因子,其昼夜节律性波动受时钟基因调控。当生物节律紊乱时,NAD⁺峰值浓度会显著下降,大大削弱细胞能量稳态的维持能力[9]。
03 更年期睡眠障碍:雌激素撤退引发的“多重打击”
女性睡眠困难通常始于绝经过渡期,绝经后患病率增加,自我报告的睡眠问题发生率为40%-56%[10],其主要病理机制涉及:
雌激素受体重塑:雌激素撤退导致大脑视前区GAT-1 GABA转运蛋白基因转录降低,从而减少细胞外GABA浓度,增加夜间觉醒风险[11]。
血管舒缩症状:约85% 的更年期女性有潮热症状,潮热发作时,核心体温会发生急速小范围波动,从而影响睡眠周期[12]。
04 情绪-睡眠负反馈循环:焦虑抑郁与睡眠障碍“如影随形”
焦虑和抑郁患者常面临严重的睡眠问题,而长期睡眠障碍也会进一步增加焦虑和抑郁风险。与白班工人相比,夜班工人患抑郁症的可能性要高40%[13],二者相互影响的核心机制包括:
皮质醇节律异常:抑郁会导致激素节律,如褪黑素和皮质醇节律的振幅降低,影响大脑中基因表达的昼夜节律模式,从而导致睡眠障碍[13]。
血清素功能失调:血清素分泌也受昼夜节律控制,长期睡眠障碍易使血清素(5-HT) 神经递质功能失调,导致抑郁焦虑等不良情绪发生或加剧[14]。
二、尿石素A的“睡眠-抗衰-美肤”三重调控:白天有精力,夜晚睡得香,肌肤焕活力
01 双轴调节昼夜节律,从肠道到全身的时钟同步
尿石素A的独特优势在于其对肠道-全身节律轴的双向调控:
肠道屏障节律修复:昼夜节律对维持肠道稳态及免疫功能起决定性作用。尿石素A可通过调控肠道上皮细胞中核心时钟基因的表达节律,逆转炎症诱导的时钟基因与紧密连接蛋白节律紊乱。在动物模型中,尿石素A不仅恢复了小鼠结肠组织中紧密连接蛋白(Clnd1, Clnd4) 和时钟基因(BMAL1, PER2) 的正常表达节律,还有效调节下丘脑视交叉上核(SCN) 的中枢时钟系统[15]。
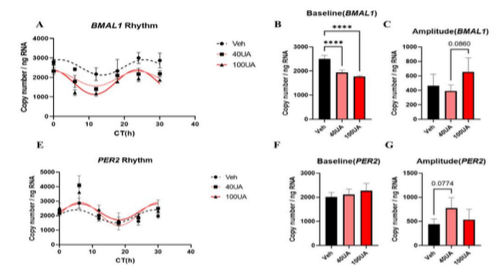
衰老细胞节律重编程:昼夜节律时钟精准调控生物体的多项生理活动,而衰老进程会削弱其时间精度与稳健性,表现为基因振荡的节律延长、振幅衰减。在衰老及增殖状态的TIG-3细胞模型中,尿石素A可显著增强BMAL1启动子驱动的荧光素酶振荡振幅,衰老细胞的振幅提升达约4倍,且呈剂量依赖性[16],提示其对衰老细胞的节律功能具有深度修复作用。
02 增强NAD+内源合成能力,促进细胞能量代谢
研究表明,尿石素A可以显著提升细胞NAD+水平,促进细胞能量代谢,帮助提升日间精力。动物实验中,补充尿石素A后,小鼠体内的NAD+水平显著提升50%,且其提升效能相当于5倍剂量的NR[17]。
值得关注的是,尿石素A对NAD+的提升不同于外源性前体补充,而是通过激活SIRT1-NAMPT通路,从源头增强NAD+的内源性合成能力[17]。这种增强自然代谢的机制,为长期服用的安全性提供了理论支撑。
03 改善睡眠剥夺性疲劳,提升日间生理机能
在睡眠剥夺小鼠模型中,尿石素A展现出优于咖啡因的抗疲劳特性。补充尿石素A后,睡眠剥夺小鼠的握力相较于未补充组提升了35%(咖啡因组仅12%)。在评估小鼠的平衡能力和运动耐力的转棒实验(ROTA-ROD) 中,补充尿石素A的小鼠感受到疲劳的时间大幅延长,改善幅度约为100%,同时还改善了睡眠剥夺小鼠的肠道菌群失调[18]。
04 睡出好皮肤,昼夜节律驱动的皮肤年轻通路
睡眠是皮肤的“天然美容剂”,其对皮肤的影响本质上是昼夜节律、激素平衡、屏障功能共同作用的结果。长期睡眠不足会加速皮肤衰老。对于现代人而言,将“睡出好皮肤”纳入健康管理,或许比任何昂贵护肤品都更具性价比。
夜间是皮肤自我修复的黄金时段,从机制上看,尿石素A可增强皮肤成纤维细胞BMAL1节律振幅,提升胶原蛋白合成相关基因(如COL1A1) 的表达,从而促进受损屏障修复与弹性纤维再生。

三、尿石素A开启睡眠与抗衰实证临床研究
01 睡眠质量临床:解码衰老与睡眠的交互机制
邦尚健康于2025年初启动的尿石素A睡眠质量干预临床研究(美国临床注册号 #NCT06990256),旨在从衰老生物学视角探索睡眠障碍的解决路径。
该项随机对照研究预计纳入80名45-70岁受试者,采用四盲设计(受试者、医护人员、研究者、评估者均设盲),设置尿石素A组、非瑟酮组、联合组及淀粉安慰剂组,进行12周干预。首次系统性评估尿石素A对昼夜节律重整及衰老相关睡眠障碍的干预潜力。
02 临床核心研究设计:
入组标准:睡眠质量受损但未达病理诊断的亚临床人群(PSQI评分 > 5分),排除咖啡因/酒精依赖者,确保干预效果的纯粹性。
多维度评估:
主观指标:睡眠质量评分、昼夜类型问卷(晨型/夜型倾向)、日间功能障碍量表;
客观指标:体动记录仪连续监测、多导睡眠图分析;
生物标志物:NAD+水平、DNA甲基化年龄、炎症因子(血浆白细胞介素)、皮质醇水平、节律蛋白、胰岛素抵抗指数、免疫球蛋白水平等。
“我们不仅关注睡眠时长与碎片化程度,更希望通过表观遗传时钟、代谢稳态等指标,揭示睡眠障碍与衰老进程的因果关系。” 项目负责人表示,“尿石素A与非瑟酮的联合用药设计,旨在探索‘昼夜节律调节 + 衰老细胞清除’的协同效应,这或将为更年期睡眠障碍等复杂场景提供新方案。”
四、邦尚健康的科学承诺:从“原料创新”到“健康生态”
作为中国高纯度尿石素A生产企业,邦尚健康的研发路径始终遵循“原料科学 - 机制研究 - 临床转化”的全链条布局。我们正面向全球招募临床合作伙伴,欢迎学术界、产业界共同探索尿石素A在睡眠健康、细胞抗衰等更多领域的应用潜力。
当“抗衰老”从消费主义叙事转向科学理性,邦尚健康以尿石素A为支点,撬动的不仅是单一成分的市场价值,更是整个行业对“证据为本”的回归。从皮肤到睡眠,从分子机制到临床终点,未来的抗衰解决方案,必须是机制清晰、数据明确、场景精准的系统性方案。
参考文献:
[1] Luis San, Belén Arranz, The Night and Day Challenge of Sleep Disorders and Insomnia: A Narrative Review. Actas Esp Psiquiatr, 2024 Feb 5;52(1):45-56.
[2] Bhagavan, S. M., & Sahota, P. K. (2021). Sleep Fragmentation and Atherosclerosis: is There a Relationship?. Missouri medicine, 118(3), 272–276.
[3] Wang Junxiu, Zhang Yan, Li Yanze. China Sleep Research Report[M]. Social Sciences Academic Press, 2025.
[4] Feeney, S. P., McCarthy, J. M., Petruconis, C. R., & Tudor, J. C. (2025). Sleep loss is a metabolic disorder. Science signaling, 18(881), eadp9358.
[5] Carreras, A., Zhang, S. X., Peris, E., Qiao, Z., Gileles-Hillel, A., Li, R. C., Wang, Y., & Gozal, D. (2014). Chronic sleep fragmentation induces endothelial dysfunction and structural vascular changes in mice. Sleep, 37(11), 1817–1824.
[6] Bonmati-Carrion, M. A., Arguelles-Prieto, R., Martinez-Madrid, M. J., Reiter, R., Hardeland, R., Rol, M. A., & Madrid, J. A. (2014). Protecting the melatonin rhythm through circadian healthy light exposure. International journal of molecular sciences, 15(12), 23448–23500.
[7] Boivin, D. B., Boudreau, P., & Kosmadopoulos, A. (2022). Disturbance of the Circadian System in Shift Work and Its Health Impact. Journal of biological rhythms, 37(1), 3–28.
[8] Mosure, S. A., Wilson, A. N., & Solt, L. A. (2022). Targeting Nuclear Receptors for TH17-Mediated Inflammation: REV-ERBerations of Circadian Rhythm and Metabolism. Immunometabolism, 4(2), e220006.
[9] Yang, Z., Zarbl, H., Kong, B., Taylor, R., Black, K., Kipen, H., Basaly, V., Fang, M., & Guo, G. L. (2024). Liver-gut axis signaling regulates circadian energy metabolism in shift workers. FASEB journal : official publication of the Federation of American Societies for Experimental Biology, 38(22), e70203.
[10] Kravitz, H. M., Ganz, P. A., Bromberger, J., Powell, L. H., Sutton-Tyrrell, K., & Meyer, P. M. (2003). Sleep difficulty in women at midlife: a community survey of sleep and the menopausal transition. Menopause (New York, N.Y.), 10(1), 19–28.
[11] Herbison A. E. (1997). Estrogen regulation of GABA transmission in rat preoptic area. Brain research bulletin, 44(4), 321–326.
[12] Santoro, N., Epperson, C. N., & Mathews, S. B. (2015). Menopausal Symptoms and Their Management. Endocrinology and metabolism clinics of North America, 44(3), 497–515.
[13] Walker, W. H., 2nd, Walton, J. C., DeVries, A. C., & Nelson, R. J. (2020). Circadian rhythm disruption and mental health. Translational psychiatry, 10(1), 28.
[14] Pourhamzeh, M., Moravej, F. G., Arabi, M., Shahriari, E., Mehrabi, S., Ward, R., Ahadi, R., & Joghataei, M. T. (2022). The Roles of Serotonin in Neuropsychiatric Disorders. Cellular and molecular neurobiology, 42(6), 1671–1692.
[15] Yao Du, Xinyue Chen et al. Effect of Urolithin A on the Improvement of Circadian Rhythm Dysregulation in Intestinal Barrier Induced by Inflammation. Nutrients 2024, 16, 2263.
[16] Rassul Kuatov, Jiro Takano et al. Urolithin A Modulates PER2 Degradation via SIRT1 andEnhances the Amplitude of Circadian Clocks in HumanSenescent Cells. Nutrients 2025, 17, 20.】
[17] Ghosh Nandini, et al. Urolithin A augments angiogenic pathways in skeletal muscle by bolstering NAD+ and SIRT1. Sci Rep. 2020 Nov 19;10(1):20184.
[18] Hongkang Zhu, Haotian Zhao et al. Urolithin A Ameliorates Athletic Ability and Intestinal Microbiota in Sleep Deprivation from the Perspective of the Gut-Muscle Axi. Mol Nutr Food Res. 2024 Apr;68(7):e2300599.
声明:*此文章中全部内容仅为一般性参考,仅为营养健康产业从业者提供信息参考服务;涉及功效相关描述均有对应的数据支持,并不代表针对消费者的宣称和指导;涉及到的保健食品、功能性食品等,不是药品,不能替代药物,读者不应在缺乏具体专业建议的情况下,擅自采取行动。




































 发布时间:2025-12-26
发布时间:2025-12-26
 分享:
分享:










 + 86 (0731) 8279-1134
+ 86 (0731) 8279-1134
 sales@bonerge.com
sales@bonerge.com