一、迟到 30 年的诺奖认可,解锁免疫调控新范式
2025年10月7日,诺贝尔生理学或医学奖授予坂口志文、Mary Brunkow和 Fred Ramsdell,表彰三人发现调节性T细胞(Treg)及FOXP3基因在免疫耐受中的关键作用——这是一个迟到了30年的认可,彻底改写了免疫治疗的核心逻辑,也为全球3.8亿自身免疫病患者带来免疫平衡调控的新希望。
过去半个世纪,医学界对免疫系统的认知陷入“越强越好”的误区:疫苗激活免疫、抗体药物增强免疫、免疫疗法唤醒抗癌细胞,这套思路推动全球免疫治疗市场从2015年的430亿美元跃升至2024年的2870亿美元[1]。然而硬币的反面早已失控,免疫失衡引发的健康危机持续升级,倒逼行业重新审视免疫平衡的价值。
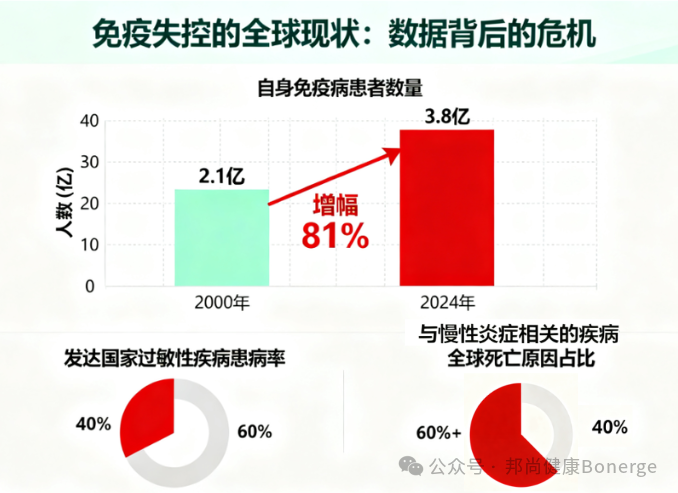
《柳叶刀》2024年全球疾病负担报告显示,自身免疫性疾病患者从2000年的2.1亿增至2024年的3.8亿,增幅达81%;发达国家过敏性疾病患病率突破40%;慢性炎症相关疾病更是占据全球死亡原因的60%以上[2]。
问题的核心,藏在坂口志文1995年的实验中:免疫系统既要“油门”(免疫激活),更要“刹车”(免疫调控),二者失衡便会诱发自身免疫病[3]。
他发现的调节性T细胞(Treg),是免疫系统的专职“调控者”——不直接杀敌,专司叫停过度免疫反应,维系免疫平衡;而FOXP3基因,正是这套刹车系统的总开关。一旦FOXP3基因失灵,免疫细胞会陷入无差别攻击,破坏自身组织,这正是自身免疫病的根源[4]。
这一发现正释放巨大医学与商业价值:2023年全球至少12款靶向Treg的药物进入临床试验,覆盖移植排斥、炎症性肠病、类风湿关节炎等自身免疫相关领域,辉瑞、诺华、再生元等药企纷纷布局。但更深层的变革在于,医学界终于正视“免疫平衡”的核心价值——免疫治疗的下一站,是精准调控,而非盲目增强。
尿石素A与非瑟酮两种天然分子的出现,提供了免疫平衡的营养干预思路:通过修复免疫系统自身“刹车”功能,实现系统自我修复,而非依赖药物强行压制,这也是诺奖背后最深刻的启示,为自身免疫病干预开辟了新路径。
二、从细胞能量到衰老清理:Treg功能重建的双轨策略
能量衰竭:Treg失能的核心诱因
调节性T细胞(Treg)功能衰退,本质是细胞内部的能量危机,而Treg功能异常正是免疫失衡的关键环节。与直觉相反,免疫调控比免疫攻击更耗能:Treg需持续合成抑制性细胞因子、高表达调控受体、在组织间频繁迁移,每一项都是能量密集型任务,其维持抑制功能所需的ATP消耗,高于同等效应T细胞[5]。
随年龄增长与氧化应激累积,细胞能量代谢效率下降,ATP产出锐减。研究表明,60岁以上人群的Treg细胞能量代谢水平显著下降,直接导致免疫耐受能力衰退,加剧免疫失衡,增加自身免疫病发病风险[6]。因此,修复细胞能量代谢,成为重建Treg功能、恢复免疫平衡的关键突破口。
尿石素A:细胞能量与代谢节律的修复者,助力免疫平衡
尿石素A是肠道菌群代谢鞣花酸产生的天然分子,核心作用是促进NAD+/NADH循环、调节细胞生物节律,系统性改善细胞能量状态,为Treg功能修复提供动力,助力免疫平衡重建,适配自身免疫病的营养干预需求。
NAD+是细胞代谢与能量稳态的核心辅酶,参与氧化还原反应与DNA修复。研究证实,补充尿石素A可显著提升体内NAD+水平,增幅达50%,效果堪比5倍剂量的NR(烟酰胺核糖)[7]。与外源性补充前体不同,尿石素A通过激活SIRT1-NAMPT通路,增强NAD+内源性合成能力[7],从源头强化细胞代谢,兼顾长期使用安全性,为免疫平衡调控提供持久支撑。
昼夜节律稳定是免疫平衡的重要保障,而衰老会导致节律振荡减弱、基因表达紊乱,间接影响Treg功能。在衰老细胞模型中,尿石素A可将生物钟振幅提升4倍,且呈剂量依赖,展现出强大的衰老细胞节律修复能力[8],为Treg功能稳定筑牢基础。
临床转化持续提速:2022年《JAMA Network Open》随机对照试验显示,每日补充500mg尿石素A,4个月后受试者Treg/Th17比例显著改善,标志着免疫平衡向健康状态回归[9]。目前市场核心挑战是仅40%人群的肠道菌群可将鞣花酸转化为尿石素A,推动了高纯度尿石素A原料发展——邦尚推出的StanYouth®尿石素A,纯度达99%以上,兼顾纯净度与安全性,为免疫平衡干预提供可靠原料支持。
非瑟酮:精准清除衰老细胞,优化免疫平衡微环境
如果说尿石素A解决Treg的“内部供电”问题,非瑟酮则聚焦“外部环境优化”——清除衰老细胞,阻断其对Treg功能的抑制,为免疫平衡扫清障碍,与尿石素A形成协同调控效应。
衰老细胞(僵尸细胞)虽仅占组织细胞的1%-5%,却会通过旁分泌释放50余种促炎因子、蛋白酶和生长因子(即SASP衰老相关分泌表型),形成慢性炎症微环境,打破免疫平衡。研究证实,SASP中的IL-1α、IL-6等因子会直接抑制Treg分化与功能,同时促进Th17等促炎细胞增殖,这是自身免疫病与慢性炎症的共同诱因[10]。
非瑟酮是目前已知最强效的天然衰老细胞清除剂之一,为免疫平衡调控提供重要助力。梅奥诊所2018年发表于《EBioMedicine》的研究,从10种候选化合物中筛选确认,非瑟酮清除衰老细胞效率最高,且对正常细胞无毒性[11],适合长期用于免疫平衡干预。
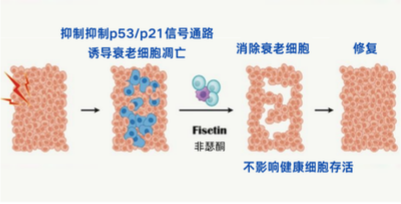
其作用机制清晰:通过抑制PI3K/AKT和BCL-2家族蛋白,特异性诱导衰老细胞凋亡,不影响健康细胞存活。动物实验证实,间歇性给药可清除50%-70%的衰老细胞,显著恢复Treg功能,重构免疫平衡微环境。
人体试验已逐步推进:梅奥诊所针对慢性肾病患者的II期试验初步结果显示,20mg/kg剂量非瑟酮间歇给药安全性良好,部分患者肾功能指标与炎症水平均有改善,间接印证了其调控免疫平衡、缓解慢性炎症的潜力。目前非瑟酮的核心挑战是口服生物利用度较低(<5%),相关制剂技术正持续优化[12]。
三、协同增效:从分子组合到免疫平衡系统重建
尿石素A与非瑟酮的联合使用,遵循系统生物学思维,不追求单点突破,而是多层面协同调控免疫平衡:尿石素A修复Treg细胞内能量代谢与节律,为其功能发挥提供支撑;非瑟酮清除衰老细胞、阻断SASP介导的慢性炎症,优化Treg工作环境,两者结合有望实现“1+1>2”的协同效应,高效重建免疫平衡。
2023年《前沿免疫学》综述指出[13],这种双分子联合干预的理论基础坚实,虽大规模人体数据仍需完善,但现有研究已展现出广阔的应用前景,为自身免疫病、慢性炎症的免疫平衡干预提供了新路径。
这并非传统营养学的回归,而是精准医学向系统修复的延伸。未来的免疫干预,将突破单一靶点药物开发的局限,融合个体代谢状态、衰老负荷与菌群特征,形成整合药物、营养与生活方式的个性化免疫平衡管理方案,适配更多自身免疫病患者需求。
尿石素A与非瑟酮的研究,不仅验证了天然分子调控免疫平衡的潜力,更标志着免疫治疗的范式转变:用生物学智慧修复免疫系统本身,而非仅用化学手段压制症状。这正是诺奖留给行业的核心思考,也为全球3.8亿自身免疫病患者点亮了免疫平衡调控的新希望。
参考来源
[1]全球免疫治疗药物市场研究报告, WISE GUY REPORTS, 13 September, 2025.
[2]Global burden of 288 causes of death and life expectancy decomposition in 204 countries and territories and 811 subnational locations, 1990-2021: a systematic analysis for the Global Burden of Disease Study 2021. Lancet. 2024 May 18;403(10440):2100-2132.
[3]Sakaguchi S, Sakaguchi N, et al. Immunologic self-tolerance maintained by activated T cells expressing IL-2 receptor alpha-chains (CD25). Breakdown of a single mechanism of self-tolerance causes various autoimmune diseases. Journal of Immunology. 1995;155(3):1151-1164.
[4]Bennett CL, et al. The immune dysregulation, polyendocrinopathy, enteropathy, X-linked syndrome (IPEX) is caused by mutations of FOXP3. Nature Genetics. 2001;27(1):20-21.
[5]Angelin A, et al. Foxp3 Reprograms T Cell Metabolism to Function in Low-Glucose, High-Lactate Environments. Cell Metabolism. 2017;25(6):1282-1293.e7.
[6]Jappreet Singh Gill, Benu Bansal, et, al. Mitochondrial Oxidative Stress Regulates FOXP3+ T-Cell Activity and CD4-Mediated Inflammation in Older Adults with Frailty. Int. J. Mol. Sci. 2024, 25, 6235.
[7]Kuatov R, Takano J, et al. Urolithin A Modulates PER2 Degradation via SIRT1 and Enhances the Amplitude of Circadian Clocks in Human Senescent Cells. Nutrients. 2025; 17(1):20.
[8]Ghosh N, Das A, Biswas N, et al. Urolithin A augments angiogenic pathways in skeletal muscle by bolstering NAD+ and SIRT1. Sci Rep. 2020;10(1):20184.
[9]Liu S, et al. Effect of Urolithin A Supplementation on Muscle Endurance and Mitochondrial Health in Older Adults: A Randomized Clinical Trial. JAMA Network Open. 2022;5(1):e2144279.
[10]Jingjing Luo, Tongxu Sun, et al.
[11]Yousefzadeh MJ, et al. Fisetin is a senotherapeutic that extends health and lifespan. EBioMedicine. 2018;36:18-28.
[12]ClinicalTrials.gov Identifier: NCT03675724, Senolytic Therapy to Modulate Progression of Alzheimer's Disease (SToMP-AD).
[13]Aoya Han, Tingting Peng, et al. Mitochondrial-regulated Tregs: potential therapeutic targets for autoimmune diseases of the central nervous system. Front. Immunol., 12 December 2023.
声明:*此文章中全部内容仅为一般性参考,仅为营养健康产业从业者提供信息参考服务;涉及功效相关描述均有对应的数据支持,并不代表针对消费者的宣称和指导;涉及到的保健食品、功能性食品等,不是药品,不能替代药物,读者不应在缺乏具体专业建议的情况下,擅自采取行动。




































 发布时间:2026-01-16
发布时间:2026-01-16
 分享:
分享:











 + 86 (0731) 8279-1134
+ 86 (0731) 8279-1134
 sales@bonerge.com
sales@bonerge.com