导语:一瓶宣称“脂质体包裹”的NAD+补充剂售价动辄上千元,却可能零有效成分!
2025年3月,行业头部公司发布的检测报告,彻底撕开NAD+保健品市场的华丽外衣,曝光脂质体技术滥用乱象——消费者高价买单,或许只是为“营销噱头”付费。
一、Niagen检测报告引爆:NAD+市场的残酷真相
1. 被神化的NAD+与失控的市场
NAD+(烟酰胺腺嘌呤二核苷酸)是细胞能量代谢与DNA修复的核心辅酶,随年龄增长含量下降,成为抗衰保健品市场“明星成分”,口服、含片、注射类NAD+补充剂层出不穷,定价居高不下。
美国营养补剂头部企业Niagen Bioscience于2025年3月发布报告,针对亚马逊平台21款热销NAD+补充剂开展检测,揭露触目惊心的行业现状,刷新大众对NAD+产品的认知:
合格率仅24%:仅5款硬胶囊NAD+补充剂达到或超出标签标注含量,多数产品未达标;
近六成严重造假:12款产品(占比57%)NAD+含量不足标签的1%,其中11款完全未检出NAD+;
脂质体光环彻底破碎:11款标榜“脂质体”技术的NAD+产品成重灾区——8款软胶囊NAD+含量为零,剩余3款虽检出NAD+,但其“脂质体提升吸收”的核心宣传,缺乏可靠科学依据支撑。
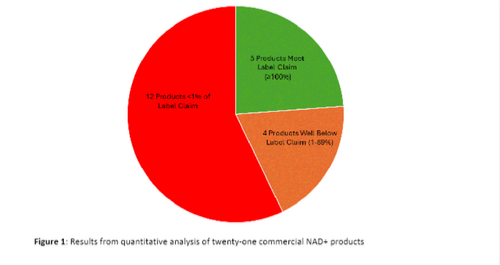
图源Niagen报告
2. 科学困局:口服NAD+有效性存疑
报告同步指出核心科学难题:即便NAD+补充剂含足量有效成分,口服或静脉注射能否有效提升细胞内NAD+水平、产生明确健康益处,目前缺乏充分严谨的临床证据。因NAD+分子大且带电荷,难以穿透细胞膜被高效利用,科学界普遍认可,补充NAD+前体(如NR、NMN)是更可行的提升路径。
二、脂质体技术:科学原理与核心价值
11款脂质体NAD+产品集体翻车绝非偶然,背后是市场对脂质体技术的滥用与信任危机。厘清乱象前,先明确脂质体技术的真实科学价值与应用门槛。
1. 脂质体:细胞膜的仿生设计优势
脂质体是磷脂双分子层构成的微囊泡,结构仿生细胞膜,是高端给药与活性成分递送的核心技术,核心优势集中在四点:
保护活性成分:避免易降解成分在消化道被破坏,留存成分活性;
提升溶解性:改善难溶性成分在胃肠道的溶解效果,突破吸收瓶颈;
促进高效吸收:通过模拟细胞膜融合或细胞摄取机制,助力成分穿透肠壁等生物屏障;
实现缓释长效:黏附于肠黏膜延长滞留时间,缓慢释放活性物质,维持稳定血药浓度。
2. 脂质体技术落地的关键前提
脂质体的优势并非简单混合就能实现,其落地依赖精密技术,核心取决于三点:
科学配方配比:需精准搭配磷脂、胆固醇(稳定膜结构)与活性成分,药物/脂质比通常为1:5至1:20,对应有效成分含量4.76%~16.7%,比例失衡会导致包裹失败或结构不稳定;
先进制备工艺:涉及脂质体形成、成分装载、粒径控制等精细步骤,需严控工艺参数,保障批间一致性与产品品质;
严格质量表征:需通过专业手段检测核心指标,包括包封率(>70%为有效标准,需用超速离心法等专业检测)、Zeta电位(绝对值>30mV保障稳定性)、粒径(100-200nm最优,需用动态光散射法测定)及外观形态(透射电镜下呈“暗-亮-暗”三层单位膜结构)。

脂质体结构TEM图像记录,其为多层结构脂质体,尺寸在 100–200 纳米范围内
三、脂质体NAD+:科技外衣下的造假重灾区
Niagen检测中11款脂质体NAD+产品几乎全军覆没,暴露行业在脂质体技术应用中的系统性漏洞,虚假宣传与技术滥用问题突出:
包封率形同虚设:厂商极少公布包封率数据,未检出NAD+的产品多为包封率极低或未形成有效脂质体结构,主流脂质体NAD+原料包封率仅3%~7%;
配方比例严重失衡:NAD+为亲水性大分子,需特定磷脂与工艺才能包裹,部分厂商将“40%以上高含量NAD+”作为卖点,违背脂质体技术原理(活性成分含量超20%即难实现有效包裹);
制备工艺极其粗糙:多数脂质体NAD+原料仅为简单粉碎混合,缺乏完整开发流程,且软胶囊剂型以油脂为载体,适配脂溶性成分,与水溶性NAD+本质适配性极差;
稳定性完全未达标:脂质体产品需保障体系稳定性(Zeta电位)与储存稳定性,但市场上无厂商开展相关研究,同类脂质体产品(水飞蓟、姜黄、谷胱甘肽、维生素C脂质体等)均存在此问题;
宣传夸大无验证:少数检出NAD+的产品,其“脂质体提升吸收”的宣称缺乏生物利用度研究与人体临床试验支撑,脂质体沦为掩盖产品无效、低质的营销遮羞布。
脂质体技术的乱象远不止于NAD+补充剂,如何识破脂质体营销话术、辨别产品真伪,成为消费者的必修课,也亟待行业完善规范、重建信任。
参考来源:
[1] Niagen Bioscience, Inc. Quantitative Analysis Report on Consumer Products Containing Nicotinamide Adenine Dinucleotide (NAD+). March 2025.
[2] Imai, S. I., & Guarente, L. NAD+ and sirtuins in aging and disease. Trends in Cell Biology. (2014).
[3] Yoshino, J., Baur, J. A., & Imai, S. I. NAD+ Intermediates: The Biology and Therapeutic Potential of NMN and NR. Cell Metabolism. (2018).
[4] Sercombe, L., et al. Advances and Challenges of Liposome Assisted Drug Delivery. Frontiers in Pharmacology. (2015).
[5] Laouini, A., et al. Preparation, Characterization and Applications of Liposomes: State of the Art. Journal of Colloid Science and Biotechnology (2012).
[6] Fan, Y., Marioli, M., & Zhang, K. Analytical characterization of liposomes and other lipid nanoparticles for drug delivery. Journal of Pharmaceutical and Biomedical Analysis. (2021).
[7] Chountoulesi, M., et al. The significance of drug-to-lipid ratio to the development of optimized liposomal formulation. Journal of Liposome Research. (2018).
[8] Géza Hegedűs, et al. Liposomal Formulation of Botanical Extracts may Enhance Yield Triggering PR Genes and Phenylpropanoid Pathway in Barley (Hordeum vulgare). Plants (Basel). 2022 Nov 3;11(21):2969.
声明:*此文章中全部内容仅为一般性参考,仅为营养健康产业从业者提供信息参考服务;涉及功效相关描述均有对应的数据支持,并不代表针对消费者的宣称和指导;涉及到的保健食品、功能性食品等,不是药品,不能替代药物,读者不应在缺乏具体专业建议的情况下,擅自采取行动。




































 发布时间:2026-01-09
发布时间:2026-01-09
 分享:
分享:










 + 86 (0731) 8279-1134
+ 86 (0731) 8279-1134
 sales@bonerge.com
sales@bonerge.com